KRAS新药Adagrasib治疗肺癌临床数据及不良反应
2020年10月27日,《OncLive》公布了一项在第32届EORTC-NCI-AACR(欧洲癌症研究与治疗组织、美国国家癌症研究院、美国癌症研究协会)国际分子靶标与癌症治疗学研讨会上提出的I/II期 KRYSTAL-1试验(NCT0)的结果,评估了 Adagrasib在具有KRAS G12C突变的晚期或转移性实体瘤患者中的治疗效果和安全性。
Adagrasib是在研的KRAS G12C共价抑制剂,不可逆且选择性地结合至KRAS G12C并将其锁定在非活性状态,具有较长的半衰期,以实现持久和连续的KRAS抑制作用,并导致深而持久的抗肿瘤活性。

通用名:Adagrasib
代号:MRTX849
靶点:KRAS G12C
临床数据
在本研究中,研究人员开始检测Adagrasib在具有KRAS G12C突变的晚期实体肿瘤患者中安全性、耐受性、药物水平、分子效应和临床活性,这些患者先前接受过化疗和抗PD-1/PD-L1治疗。
试验的主要终点包括药物的安全性、药代动力学和临床活性。此外,探索目标包括检查药效学生物标记物和分子标记与抗肿瘤活性的相关性。
肺癌
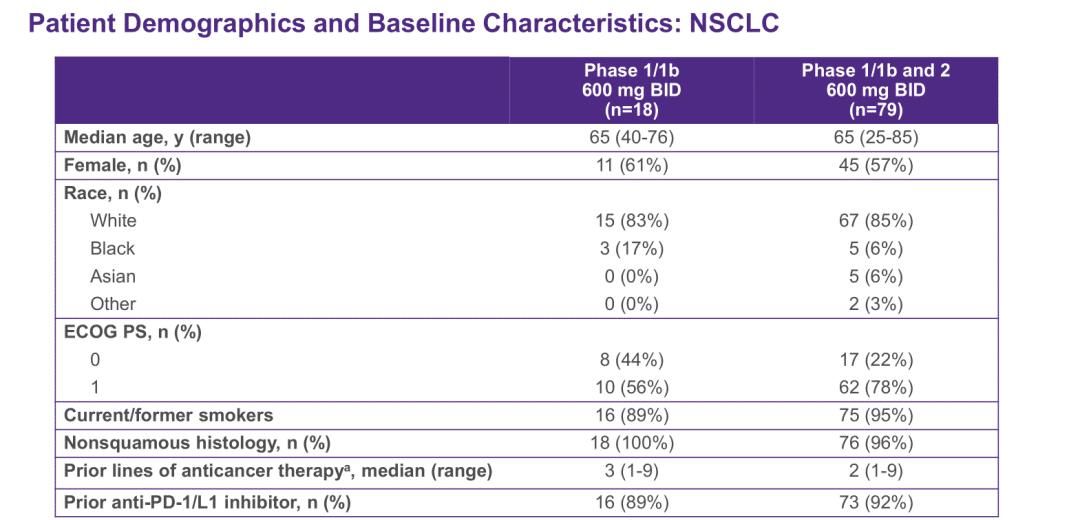
I/Ib期和II期队列(n = 79)的入组人群特征:中位年龄为65岁,57%的患者为女性,85%的患者为白种人;ECOG评分为0(22%)或2(78%);目前或曾经吸烟患者的比例为95%;96%的患者为非鳞状癌;先前接受过抗癌疗法的中位数为2;92%的患者先前接受过抗PD-1/PD-L1治疗。
I/Ib期队列(n = 18)的入组人群特征:中位年龄为65岁,61%的患者为女性,83%的患者为白种人;ECOG评分为0(44%)或2(56%);目前或曾经吸烟患者的比例为89%;100%的患者为非鳞状癌;先前接受过抗癌疗法的中位数为3;89%的患者先前接受过抗PD-1/PD-L1治疗。
研究数据显示:
在I/Ib期和II期队列中,可评估疗效的患者为51例;客观缓解率(ORR)为45%;部分缓解(PR)为45%;疾病稳定(SD)为51%,疾病进展(PD)为2%;疾病控制率(DCR)为96%;70%的应答者肿瘤缩小40%以上。
在I/Ib期队列中,可评估疗效的患者为14例,中位随访时间为9.6个月;客观缓解率(ORR)为43%;部分缓解(PR)为43%;疾病稳定(SD)为57%;疾病控制率(DCR)为100%。
案例分析
一名77岁女性,有吸烟史。于2019年4月确诊为非小细胞肺癌。NGS检测结果显示:KRAS G12C。
2019年5月-7月,患者接受Keytruda联合卡铂和培美曲塞治疗。
2019年8月-12月,继续培美曲塞治疗。
2019年11月,左额脑接受了放疗。
2020年1月- 2月,继续Keytruda治疗。同年3月,接受培美曲塞治疗,左右小脑进行放疗。
2020年5月,患者开始服用Adagrasib,600mg,每天2次。目前,患者仍在接受治疗(第7周期)。
出现的不良反应为:恶心、呕吐、腹泻、吞咽困难、贫血、皮疹、大腿不适。
14例KRAS G12C和STK11共突变患者的ORR为64%。未发现KEAP1和TP53等其它共存突变对Adagrasib的临床疗效有影响。

结直肠癌和其他实体瘤
在初步安全数据分析纳入的31例患者中,24例患者为结直肠癌(CRC),7例患者为其他实体瘤。
结直肠癌队列的入组人群特征为:中位年龄为59岁;75%的患者为白种人;ECOG评分为0(38%)或2(63%);先前接受过抗癌疗法的中位数为4。
其他实体瘤队列的入组人群特征为:中位年龄为64岁;71%的患者为白种人;ECOG评分为2(100%);肿瘤类型包括:胰腺导管腺癌(2例)、胆管癌(1例)、子宫内膜癌(1例)、卵巢癌(1例)、阑尾癌(2例);先前接受过抗癌疗法的中位数为2。
在可评估的结直肠癌患者(n=18)中,ORR为17%,SD为78%;DCR为94%;55%的患者治疗时间超过4个月。
在可评估的其他实体瘤患者(n=6)中,1例子宫内膜癌和1例胰腺癌的患者中观察到已确认的部分缓解(PRs);1例卵巢癌和1例胆管癌的患者中观察到未经证实的PRs。这6例目前仍在接受治疗。
文章来源:《中国新药与临床杂志》 网址: http://www.zgxyylczz.cn/zonghexinwen/2020/1110/384.html