两周内47个新药获批临床,国产占8成,132款药品
(人民日报健康客户端 李宣璋)据国家药监局公开资料显示,近半个月以来,4款新药申请上市、21个新药的注册办理状态有更新、47个新药获批临床、60个新药临床申请获承办。
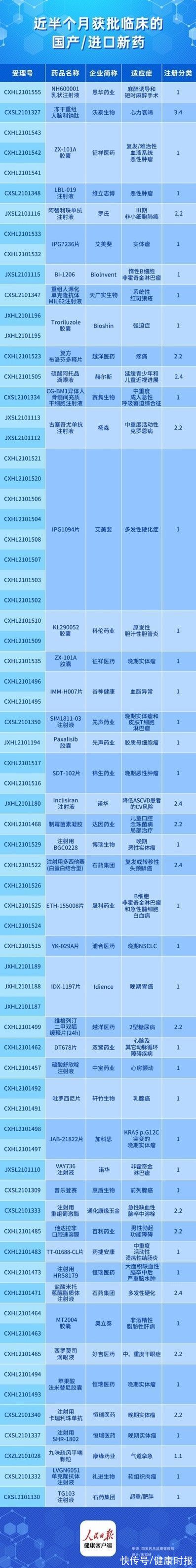
47个新药获批临床,国产占8成
健康时报记者根据国家药监局官网数据梳理发现,从11月27日至12月12日,两周时间里,47个新药获得临床试验默示许可。其中,39个品种为国产新药,8个品种为进口新药。从药品类型来看,化学药有31个、治疗用生物制品有15个、中成药有1个。39个国产新药中,1类新药有28个。
其中,恒瑞医药以4款新药获批临床领跑国内药企:注射用HRS8179为首次获批临床,该药通过减少钠离子内流,治疗大面积缺血性脑卒中后严重脑水肿,国内外尚无同类产品上市销售;苹果酸法米替尼胶囊、注射用SHR-1802及注射用卡瑞利珠单抗三款新药联合用于治疗晚期实体瘤患者。
60个新药临床申请获承办:化学药、生物制品为主流、中成药仅1个
近半个月来,60个新药的临床申请获国家药监局承办受理。其中,46个品种为国产新药,14个品种为进口新药。从药物类型来看,化学药有29个、治疗用生物制品有30个、中成药有1个。
唯一获临床申请的中成药为江苏省中医药研究院的补骨脂总苷胶囊,治疗领域为骨骼肌肉系统疾病用药。
4款新药申请上市,国内外药企平分秋色
近半个月,4个新药的上市申请获得国家药监局的承办,国内、国外药企各占一半:先声药业的注射用曲拉西利、康哲生物的甲氨蝶呤注射液(预充式)以及罗氏的注射用维博妥珠单抗、日本盐野义的芦曲泊帕片。
先声药业与G1 Therapeutics合作的曲拉西利为全球首个且唯一具有全面骨髓保护功效的CDK4/6抑制剂,是可以减少化疗导致的骨髓抑制(CIM)的一种全新疗法,曾获美国FDA“突破性疗法”认定,并于今年2月在美国上市。
此次申请的首个适应症为在接受含铂类药物联合依托泊苷方案的广泛期小细胞肺癌患者中预防性使用,以降低化疗引起的骨髓抑制的发生率。
罗氏的维博妥珠单抗(Polivy)是一种First-in-Class的抗CD79b抗体偶联药物(ADC),也是首个在国内申请上市的抗CD79b抗体偶联药物。维博妥珠单抗最早于2019年6月在美国获批上市。
21个新药的注册办理状态有更新,齐鲁有望冲刺国产第二家
据国家药监局公开资料显示,近半个月来,21个新药的注册办理状态有更新。其中,12个新药获批上市,7个新药注册办理状态变更为“在审批”,2个未被批准。
获批上市的药品中,齐鲁制药的注射用重组人促卵泡激素用于治疗不孕不育症。据米内网数据显示,2020年中国城市公立医院、县级公立医院、城市社区中心以及乡镇卫生院终端重组人促卵泡激素销售额超过12亿元。
目前国内仅有1家国产企业重组人促卵泡激素获批上市,即长春金赛药业,齐鲁有望冲刺国产第二家。
文章来源:《中国新药与临床杂志》 网址: http://www.zgxyylczz.cn/zonghexinwen/2021/1213/1241.html
上一篇:甘李药业完成新药GZR18在中国I期临床首次人体给
下一篇:没有了